HOME / SCIENCE / RAS 신호경로
RAS 신호경로

암과 RAS 신호경로
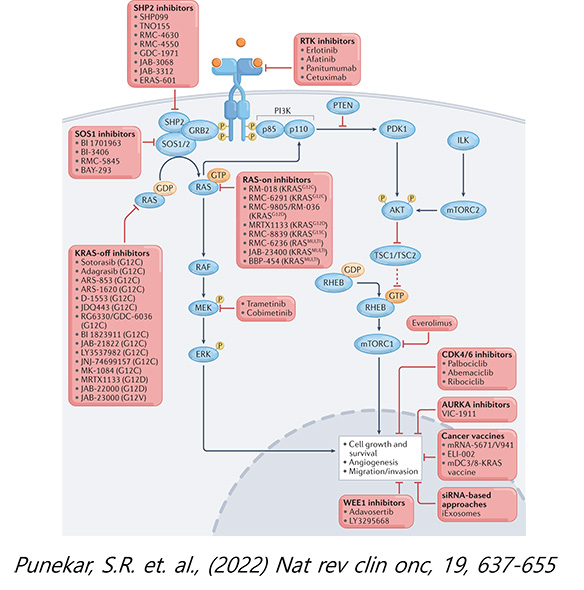
RAS GTPases는 정상적인 성장 신호 조절에 관여하는 KRAS, HRAS, NRAS 단백질을 암호화하는 3개의 유전자로, 돌연변이 획득 시 종양발생을 유도한다고 알려진 종양 유전자 (oncogene)이기도 하다. RAS 돌연변이는 전 세계 전체 암 환자의 25%에서 발견되며 특히 폐암, 대장암, 췌장암 환자에서 높은 빈도로 발견되고 있습니다. 지난 40년간 RAS 변이 암 치료제를 개발하려는 시도가 많았으나 모두 실패하여 약물 개발이 불가능한 표적이라고 평가되었습니다. 최근 KRAS 돌연변이의 14%를 차지하고 있는 KRAS G12C 변이 단백질에 직접 공유결합하여 그 기능을 억제하는 Lumakras (sotorasib, AMG510, Amgen)와 Kraziti (adagrasib, MRTX-849, Mirati)의 FDA 가속승인으로 다른 RAS 돌연변이 암종 치료제에 대한 희망과 기대가 커졌습니다.
티씨노바이오사이언스에서는 KRAS 변이암 치료제로 ULK1 저해제 (Best-in-class)와 '표적 S' 저해제 및 ‘표적 Y’저해제 (First-in-class)를 개발하고 있습니다.
합성치사 기전의 RAS 변이암 치료제, ULK1 저해제와 표적 Y 저해제
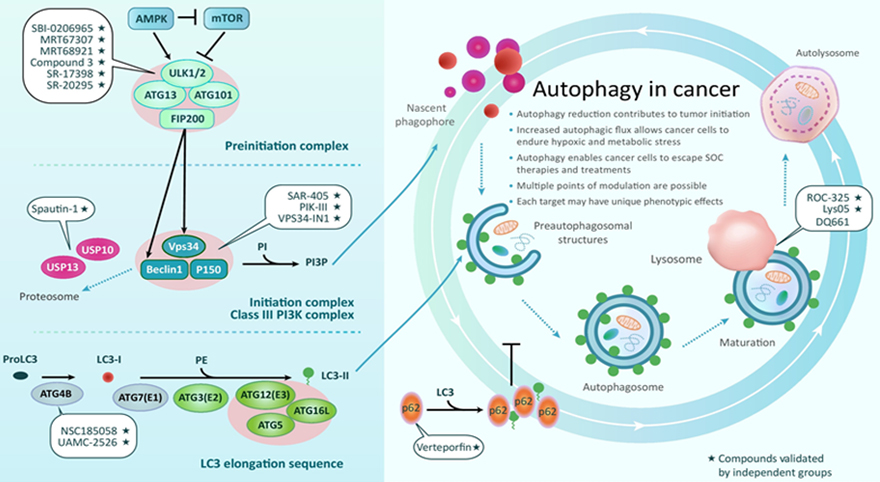
ULK1은 serine/threonine 단백질 키나아제로 에너지 결핍 (starvation), 산화작용 (oxidation) 과 같은 세포 스트레스 환경에서 자가포식 과정을 유도하는 데 관여합니다. 자가포식은 암세포의 면역 회피뿐만 아니라 생존, 약물 내성에도 중요한 역할을 하는 것으로 알려져 있습니다. 흥미롭게도, KRAS 돌연변이 암세포에서 ULK1과 MEK가 동시에 억제되었을 때, ULK1의 저해가 MEK 저해제의 항암효능을 향상하는 것으로 보고되었습니다. (2019 AACR-NCI-EORTC 포스터 발췌)
티씨노바이오사이언스에서는 KRAS 혹은 EGFR 변이암 합성치사(synthetic lethality) 약물로 ULK1 저해제/TPD (KRAS G12C or EGFR 저해제 병용)를 개발하고 있습니다. 이러한 병용치료법은 1) KRAS G12C 돌연변이 외의 다른 돌연변이 암도 적용 가능하며, 2) EGFR 치료제 저항성을 극복할 수 있으며 3) 병용 시, 기존 표적항암제의 동량 또는 더 낮은 용량에서도 개선된 치료 효과를 기대할 수 있습니다.
RAS 변이암에서 ULK1 저해제
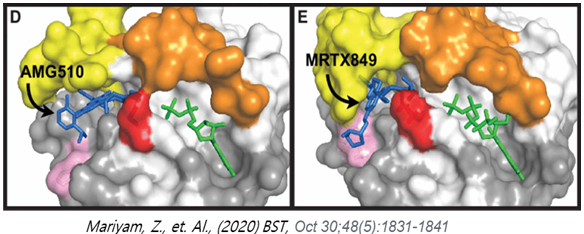
최근 G12C 변이를 가지는 KRAS 단백질에 직접 공유결합을 형성하여 활성을 억제하는 약물 Lumakras와 Krazati가 미국 FDA에서 승인되어 비소세포성 폐암 환자를 치료하는 데 사용되는 획기적인 진보가 있었습니다. 그러나, G12C 저해제는 전체 KRAS 변이암 중 14%의 환자에서 발견되는 KRAS G12C 변이암에 존재하는 시스테인(Cysteine)과 공유결합을 통해 작용하므로, 나머지 86%를 차지하는 시스테인이 없는 돌연변이의 KRAS 변이암에는 치료 효과가 없는 한계를 가지고 있습니다. 또한, 최근 논문에 따르면 (Awad MM, et al. (2021) New England Journal of medicine, 384:25), KRAS G12C 저해제 (Adagrasib, Mirati 社)에 저항성을 보이는 환자 30%에서 G12C 이외의 새로운 KRAS 돌연변이가 발생하여 내성을 유발한다고 보고되었습니다. 이러한 이유로 G12C 외의 다른 KRAS 변이암에 대한 새로운 치료제가 필요한 상황입니다.
티씨노바이오사이언스에서는 돌연변이 KRAS의 활성을 직접 저해하는 치료제로 ‘표적 S’를 개발하고 있습니다. 이러한 치료제는 의학적 미충족 수요가 큰 다른 KRAS 변이암 치료에 사용될것으로 기대됩니다.
