HOME / SCIENCE / 선천면역계
선천면역계

STING 경로 및 선천면역계
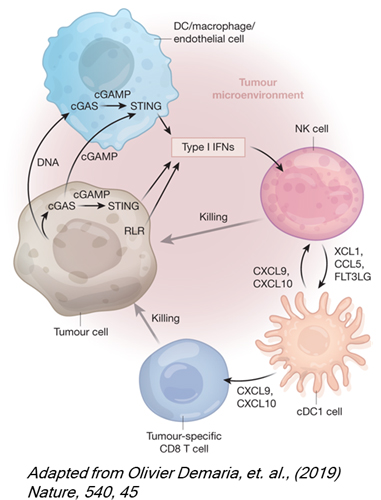
병원체 침입에 대항하는 선천면역 반응에는 7개의 신호전달체계가 관여한다고 알려졌으며 각 전달체계는 병원체에 의해 분비되는 특정한 분자 패턴을 인식합니다. STING은 소포체에 있는 막 단백질이며 세포내 DNA를 인식하여 선천면역 반응을 유도합니다. 암세포의 유전체 불안정성과 그로 인해 생성되는 세포질 내 DNA에 의한 STING 신호경로 활성화는 암세포에 대한 면역 반응을 유도하는 필수적인 경로로 알려져 있습니다. 암세포에서 cGAMP에 의한 STING의 활성화는 I형 인터페론의 생산을 유발하지만, 항암 면역 반응을 유도하기 위해서는 암세포 외부인자의 활성화가 필요한 것으로 알려져있습니다. 1세대 STING 효능제 (cGAMP의 유사체)의 낮은 반응률로 인해 임상 결과가 기대에 못 미쳤으며, 이를 극복하기 위한 노력이 지속되고 있습니다.
티씨노바이오사이언스에서는 STING 신호 경로를 조절할 수 있는 ENPP1 저해제 (Best-in-class)와 ‘표적 Z’를 타겟으로 하는 First-in-class 약물을 개발하고 있습니다.
선천면역 활성과 ENPP1 저해제
ENPP1 (Ectonucleotide pyrophosphatase/phosphodiesterase 1)은 뉴클레오티드 파이로포스파타제 및 포스포다이에스터라제 효소 활성을 가진 II형 막 단백질로써 STING 경로 조절에 중요한 역할을 하는 것으로 최근에 밝혀졌습니다. ENPP1은 종양 조직에서 면역전달물질인 cGAMP를 가수분해하여 STING 활성에 의한 인터페론 생성을 막음으로써, 암세포에 대한 선천면역 반응을 억제하는 “선천면역관문(innate immune checkpoint)” 단백질로 작용합니다. ENPP1은 많은 암종에서 과발현되어 있고, 암세포 스스로 발현을 유도하여 면역회피 반응을 일으킵니다.
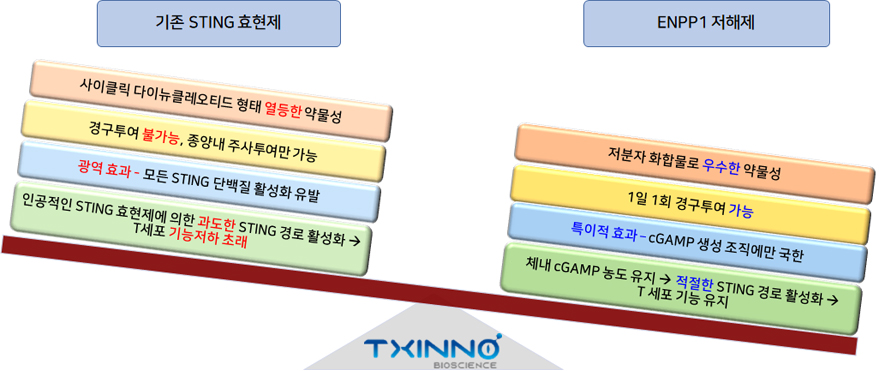
ENPP1 저해제의 장점은 다음과 같습니다. 1) 과도한 STING 활성화를 유발하는 STING 효현제와 달리 암-면역세포의 주변 cGAMP 농도에 영향을 미쳐 적절한 STING 활성화를 유지하며 2) 경구 투여 가능한 ENPP1 저해제는 현재 STING 효능제의 종양 내 주사의 한계점을 극복할 수 있습니다.
암 취약성(Cancer vulnerability)
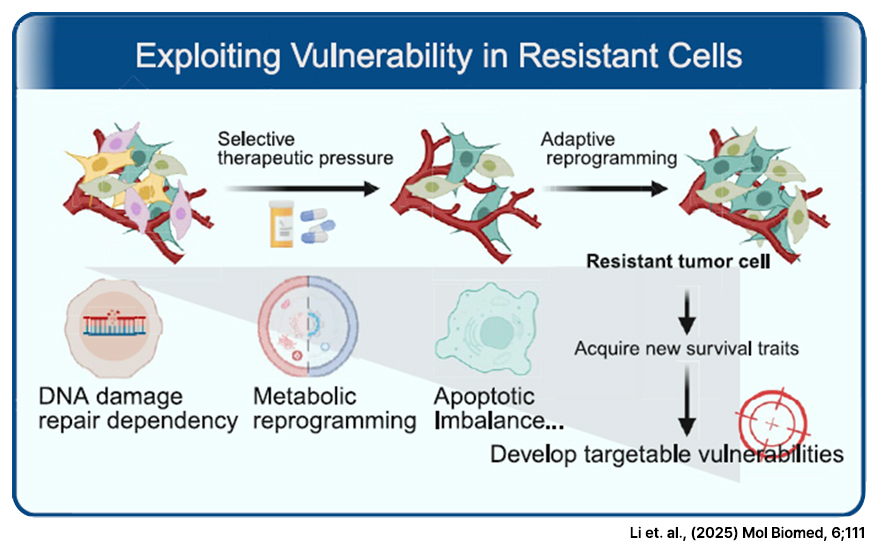
약물 내성은 진화적 선택의 결과로 약물 내성 세포는 보상 경로 활성화 또는 표현형의 변화를 통해 생존하지만, 이러한 적응은 새로운 의존성 생성하여 치료 옵션으로 활용할 수 있는 기회를 제공하기도 합니다. 이는 암 취약성(cancer vulnerability) 라고 불리며 암세포의 적응적 특성이 오히려 치명적인 약점이 되어 DNA 복구, 대사 재프로그래밍, 계통 가소성 등에 대한 암 특이적 취약성을 가지게 됨을 말합니다.
이러한 약물 내성 세포의 취약성을 표적으로 하는 암 치료전략은 단순히 세포 내 신호 전달 경로를 차단하는 것을 뛰어넘어 생물학적 진화원칙으로 획득된 취약성을 활용한 장기적인 질병 관리의 개념으로 확장시킬 수 있습니다.
티씨노바이오사이언스티씨노바이오사이언스에서는 이러한 암세포 취약성 개념을 활용하여 KRAS 변이암 치료제로 ULK1 저해제 저해제 (Best-in-class)와 ‘ULK1 TPD, ‘표적 W’ TPD 를 개발하고 있습니다.
