HOME / SCIENCE / Platforms
Platforms

플랫폼 기술 : TxLFinder™ / TxTQuantifier™
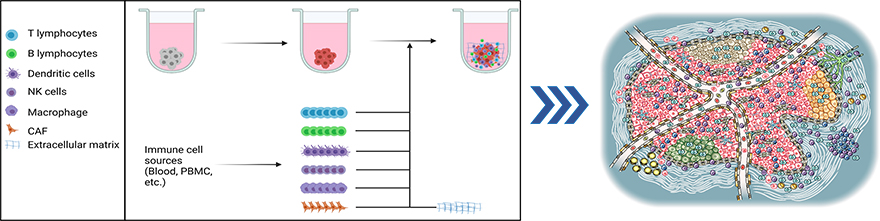
종양은 단순한 암세포의 집합체가 아니라 고유한 종양미세환경(TME) 하에서 다양한 유형의 세포로 구성된 복잡한 조직입니다. 암에 대한 이해가 깊어짐에 따라 단순히 암세포를 연구하는 것만으로는 종양미세환경에서 암세포와 다른 유형의 세포 간에 다양한 상호 작용을 (예를 들어 암세포와 면역세포에 의해 조절되는 면역 억제 환경) 완전히 이해하는데 충분하지 않습니다. 이에, 다양한 항암제를 평가하기 위한 종양미세환경을 모방한 생체 외 세포 배양 시스템의 개선을 위해 꾸준한 노력이 있었지만, 적절한 배양 평가계 구축은 개선의 여지가 남아 있습니다. 이상적인 평가계는 1) 서로 다른 세포들 조성이 균일하여 정량적 분석이 가능해야 하며, 2) 특별한 배양용기나 장비 없이 기존의 세포 배양 시설에서도 쉽게 배양 가능해야 하며, 3) 인간과 마우스 세포에 모두 적용 가능해야 합니다.
티씨노바이오사이언스에서는 이러한 문제를 해결하고 약물 개발 프로세스를 촉진하기 위해 두
가지 플랫폼 기술을 구축했습니다.
1) TxLFinder™는 마이크로 플레이트에 암 세포주 3D 입체구성체 (Spheroid)와 면역세포 (PBMC)를 공동 배양하여, 암
입체구성체로의 면역세포 침윤 여부와 동시에 항암효과를 평가할 수 있습니다.
2) TxTQuantifier™는 암 세포주, 분리된 인간 면역세포, 암 관련 섬유아세포, 지방 세포 및 세포 외 기질로 구성된 인간의
종양미세환경을 가장 가깝게 모방하기 위해 고안된 공동 배양 평가계입니다.
티씨노바이오사이언스의 TxLFinder™는 면역세포 침윤이 낮은 cold tumor에서 선천면역 항암제에 의한 면역세포 침윤의 변화, 즉 hot tumor로의 전환을 측정할 수 있는 매우 유용한 플랫폼 기술이며, 다양한 기전의 선천면역 항암제의 효능을 평가할 수 있습니다.
티씨노바이오사이언스의 TxTQuantifier™는 유사 종양미세환경에서 저분자 약물, 항체치료제 및 세포치료제의 유효성 평가와 차세대 암 표적을 찾기 위한 대용량 스크리닝 (예, CRISPR 라이브러리 스크리닝)에 활용할 수 있습니다.
인체유래 암세포주와 면역세포 공동배양 평가계 (Version 1)를 업그레이드하여 인체유래 암세포주와 암연관 섬유아세포의 공동 spheroid에 면역세포를 함께 공동배양하는 평가계 (Version 2)를 확립하여 운용하고 있습니다. 다음 단계로 종양미세환경에 존재하는 다른 종류의 세포들 (내피세포, 등등)과 세포외 기질을 추가한 평가계로 (Version 3) 업그레이드를 진행하여 좀 더 인체 종양미세환경에 근접한 평가계를 확립하고자 합니다.
플랫폼 기술 : TxBProfiler™
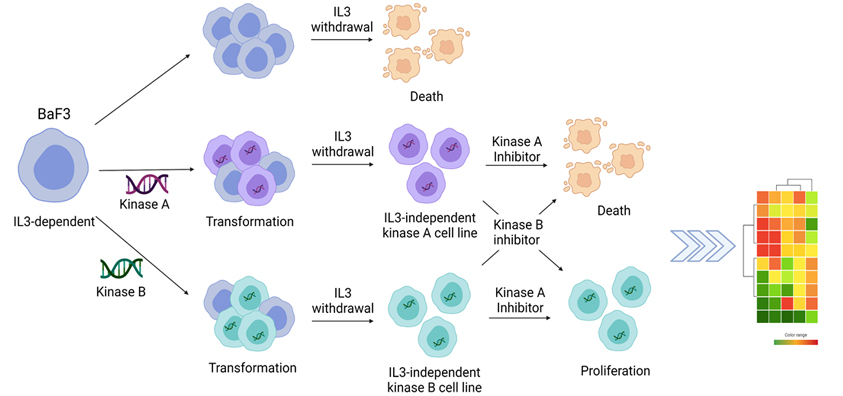
정제된 효소를 사용한 시험관내 키나아제 평가계는 지난 수십 년 동안 다양한 키나아제 저해제를 개발하는 데 필요한 기초적인 평가 방법으로 자리 잡았지만 개선하기 어려운 명백한 한계가 있습니다.
1) 분석에 사용된 ATP 농도가 세포 내부보다 낮아서 저해제의 활성이 높게 평가될 가능성이 있으며, 2) 세포 내부에서 생성되는 효소와 유사한 전사 후 변형 등의 특성을 갖도록 재조합 단백질을 정제하는 것은 여전히 어려운 과제입니다.
TxBProfiler™ 기술은 이러한 한계를 극복하기 위해 Ba/F3 세포내 유전조합으로 발현된 단일 키나아제 단백질의 활성에 의해서만 Ba/F3 세포가 IL3 독립적 증식 (IL3-independent proliferation)을 할 수 있도록 고안되어 구축되었습니다. 발현된 키나아제가 화합물에 의해 저해될 때 나타나는 성장 저해를 측정함으로써 저해제의 활성을 세포 내부에서 추정할 수 있습니다.
티씨노바이오사이언스는 약물 발굴을 위하여 현재 50여 종의 서로 다른 키나아제를 발현하는 Ba/F3 라이브러리를 확보하였으며, 신규 과제 단백질 (키나아제 또는 RAS 단백질)에 대한 Ba/F3 세포주를 추가로 개발하고 있습니다.
플랫폼 기술 : TxPchider™ - AI 기반 PROTAC 탐색 Platform
티씨노바이오사이언스 독자적인 AI 기반 PROTAC 탐색 platform 구축

인체에는 약 2만종의 단백질이 존재하고, 단백질 변형이나 특정 단백질의 과발현이 질병을 유발하기 때문에 세포는 제거해야 할 단백질에 맞춤형 표식을 붙여 분해하는 시스템을 갖추고 있습니다. 기존 표적 치료제는 특정 단백질에 결합, 확장과 기능을 억제하지만, TPD(Target Protein Degrader) 기술은 세포의 단백질 분해 시스템을 통한 표적 단백질 제거를 유도합니다. 유비퀴틴-프로테아좀 시스템(UPS)을 활용하여 단백질을 분해하는 시스템을 기반으로 하는 TPD 기술 중 대표적인 것은 프로탁(PROTAC, PROteolysis-Targeting Chimera) 기술입니다.
프로탁 기술은 기존 저해제로 접근하기 어려운 치료 불가능한(undruggable) 단백질도 제거 가능하고, 표적단백질의 촉매화 분해를 진행하므로 기존 약물 보다 사용량이 적어 고농도 약물사용에 따른 독성을 피할 수 있다는 장점을 가지고 있습니다.
티씨노바이오사이언스는 저분자 약물로 표적하기 어려운(undruggable) 단백질에 대한 치료제 개발을 위해 AI기반 프로탁 탐색 플랫폼 기술인 TxPchider 를 확보하였습니다. 해당 기술은 약물표적에 유효한 Warhead의 발굴, Linker와 E3 Ligase binder의 최적 조합 및 약물성 확보 시스템으로 효율적인 프로탁 약물 개발을 위한 AI기반 플랫폼 기술입니다.
